Bạn đang xem bài viết FeSO4 có kết tủa không? Tính chất hóa học, vật lí Hóa học 12 tại Thcslytutrongst.edu.vn bạn có thể truy cập nhanh thông tin cần thiết tại phần mục lục bài viết phía dưới.
FeSO4 hay còn gọi là sắt 2 sunfua (II) là một hợp chất hóa học quan trọng thuộc nhóm muối sunfat. Với công thức hóa học FeSO4, chất này gồm một nguyên tử sắt, một nguyên tử lưu huỳnh và bốn nguyên tử oxi. FeSO4 thường tồn tại dưới dạng các tinh thể màu xanh nhạt, có khả năng hút ẩm từ không khí.
Khi FeSO4 tiếp xúc với không khí, nó sẽ bị oxi hóa và chuyển thành Fe2(SO4)3, một chất tan trong nước. Điều này có nghĩa là trong điều kiện bình thường, FeSO4 tồn tại ở dạng không tích cực. Tuy nhiên, khi được hòa tan trong nước, FeSO4 lại tạo thành ion sắt (II) (Fe^2+) và ion sunfat (SO4^2-), cho thấy tính khử và tạo thành tinh thể kết tủa màu trắng.
FeSO4 còn có khả năng tác dụng với các chất khác, làm thay đổi tính chất của chúng. Ví dụ, khi hòa tan FeSO4 trong nước, ta thu được dung dịch có khả năng oxi hóa một số chất khác như acid sunfuric (H2SO4) và dung dịch chứa ion giả kim (Fe^3+). Đồng thời, FeSO4 cũng có thể tác dụng với dung dịch kiềm, tạo thành kết tủa không tan của sắt (II) hidroxit (Fe(OH)2).
Về mặt vật lý, FeSO4 là một chất rắn phân tử có khối lượng phân tử là 151.91 g/mol. Nhiệt độ nóng chảy của chất này là 64 °C và nhiệt độ sôi là 330 °C. Đồng thời, FeSO4 cũng có khả năng hút ẩm cao, khiến nó trở nên dễ hòa tan trong nước.
Nhờ những tính chất hóa học và vật lí đặc biệt, FeSO4 được sử dụng trong nhiều lĩnh vực như y tế, nông nghiệp và công nghiệp.
FeSO4 là một hoá chất rất quan trọng trong cuộc sống. Vậy FeSO4 có kết tủa không thì hãy theo chân Chúng Tôi tìm hiểu ngay dưới đây nhé!
FeSO4 có kết tủa không?
Trước khi đi vào chi tiết đáp án FeSO4 có kết tủa không? Bây giờ chúng ta sẽ bắt đầu với khái niệm đầu tiên FeSO4 là chất gì?
FeSO4 là chất gì?
FeSO4 hay còn được gọi phèn sắt. FeSO4 là một hợp chất muối của sắt có màu xanh. Chúng tồn tại ở 2 dạng là bột hoặc tinh thể với công thức hóa học là FeSO4.
Bình thường hóa chất này sẽ ở trạng thái ngậm nước và có công thức như sau FeSO4.7H2O.
FeSO4 có kết tủa không?
FeSO4 có kết tủa khi tác dụng với muối. Sắt II sunfat tác dụng với muối và tạo ra kết tủa.
Cân bằng phương trình Hóa học: FeSO4 + BaCl2 → BaSO4 + FeCl2.

Cấu tạo FeSO4
Sắt II sunfat FeSO4 bao gồm Fe và nhóm SO42-
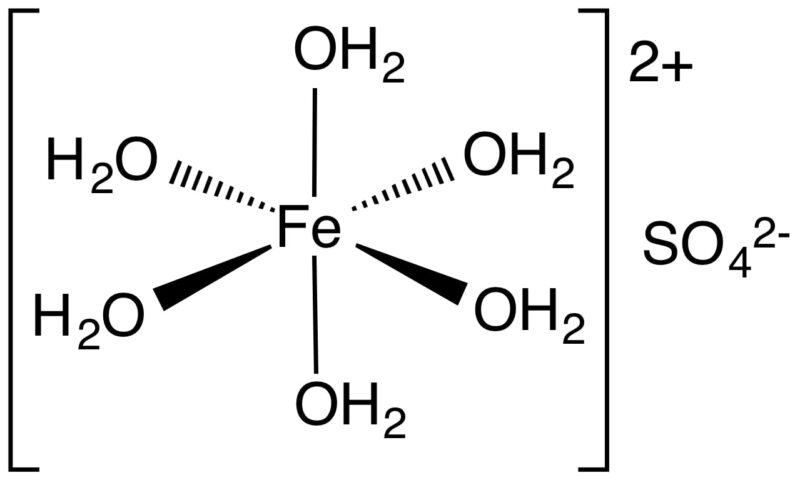
Tính chất của sắt II Sunfat FeSO4
Tính chất Vật lý của FeSO4
Một số tính chất vật lý và cách nhận biết của FeSO4:
- FeSO4 có màu sắc xanh, dạng bột hoặc phân tử và không mùi.
- Khối lượng phân tử: 151.91 g/mol (dạng khan), 278.02 g/mol (dạng ngậm 7 nước).
- Khối lượng riêng: 3.65 g/cm3 (dạng khan) và 1.859 g/cm3 (dạng ngậm 7 nước).
- Điểm nóng chảy: 680 oC (dạng khan), 60 – 64oC (dạng ngậm 7 nước).
- Hòa tan tốt trong nước (44.69 g/100ml ở 77 oC) cho dung dịch không màu, nhưng không tan trong rượu.
- Nhận biết: sử dụng dung dịch BaCl2, thấy xuất hiện kết tủa trắng:
- PTHH: FeSO4 + BaCl2 → BaSO4 + FeCl2.

Tính chất Hóa học của FeSO4
FeSO4 mang đầy đủ tính chất hóa học của muối.
- Có tính khử và tính oxi hóa:
- Tính khử: Fe2+ → Fe3+ + 1e
- Tính oxi hóa: Fe2+ + 1e → Fe
- FeSO4 mang đầy đủ tính chất hóa học của muối.
- FeSO4 tác dụng với dung dịch kiềm tạo ra 2 muối. PTHH: FeSO4 + KOH → K2SO4 + Fe(OH)2
- FeSO4 tác dụng với muối và tạo ra kết tủa. PTHH: FeSO4 + BaCl2 → BaSO4 + FeCl2
- FeSO4 mang tính khử.
- PTHH: FeSO4 + Cl2 → FeCl3 +Fe2(SO4)3
- 2FeSO4→ Fe2O3+ SO2 + SO3
- 2FeSO4 + 2H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + 2H2O
- 10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
- FeSO4 còn mang tính oxi hóa:
- PTHH: FeSO4 + Mg → MgSO4 + Fe
- 12FeSO4 + 3O2 → 4 Fe2(SO4)3 + 2Fe2O3
Điều chế FeSO4
Để điều chế FeSO4 người ta thường sử dụng 2 phương pháp sau:
- Để điều chế Sắt II sunfat FeSO4 người ta thường cho kim loại Fe dư tác dụng với axit HNO3.
- PTHH: 3Fe + 8HNO3 → 4H2O + 2NO + 3Fe(NO3)2
- Ngoài ra, cũng có thể sử dụng Fe kết hợp với CuSO4
- PTHH: Fe + CuSO4 → FeSO4 + Cu
Ứng dụng của FeSO4
Một số ứng dụng của FeSO4 trong đời sống hiện nay như:
Ứng dụng của FeSO4 trong quy trình xử lý nước
FeSO4 có vai trò làm chất keo tụ cũng như một chất dùng trong phản ứng oxi hóa khử. Mục đích để loại bỏ photphat trong nước của các nhà máy xử lý nước thải công nghiệp và đô thị.
Ứng dụng của FeSO4 trong công nghiệp nhuộm, thuộc da
FeSO4 có vai trò như một chất cố định thuốc nhuộm và được biết đến như chất tiền của các hợp chất sắt khác. FeSO4 mang tính chất là một chất khử nên được ứng dụng trong việc khử cromat trong xi măng thành các hợp chất Cr (III) ít độc hơn.
FeSO4 còn được sử dụng trong ngành dệt may để làm đen da và là thành phần tạo nên mực.
Ứng dụng của FeSO4 trong y học, y tế
Một trong những ứng dụng nổi bật của FeSO4 là trong ngành y tế:
- FeSO4 được sử dụng để củng cố thực phẩm và điều trị, ngăn ngừa thiếu máu do thiếu sắt.
- FeSO4 là một nguyên tố vi lượng quan trọng mà cơ thể cần để sản xuất các tế bào hồng cầu, giúp cơ thể bạn khỏe mạnh.
Ứng dụng của FeSO4 trong tạo màu trong công nghiệp in ấn, mực
Hiện nay, FeSO4 nó cũng được sử dụng trong nhuộm len như một chất gắn màu.
Ứng dụng của FeSO4 trong nông nghiệp, phân bón
FeSO4 dùng cải tạo chất lượng đất, hạ thấp độ pH của đất có độ kiềm cao. Giúp cây có thể tiếp cận với chất dinh dưỡng của đất
và FeSO4 còn được sử dụng để điều trị nhiễm clo sắt.
FeSO4 nó cũng được sử dụng làm chất diệt cỏ và rêu.

Những lưu ý khi sử dụng và bảo quản FeSO4
Một số lưu ý khi sử dụng và bảo quản FeSO4 để an toàn cho người sử dụng:
- FeSO4 với đặc tính dễ hút ẩm gây vón cục, đông cứng. Do đó, khi bảo quản cần chú ý để nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp và nguồn gây cháy.
- FeSO4 với đặc tính ăn mòn nên tránh dùng các vật liệu sắt, đồng, nhôm hoặc vật liệu hút ẩm để cất trữ.
- FeSO4 nên được bảo quản và lưu trữ trong các loại vật liệu như sợi thủy tinh, thép không rỉ, bao nhựa để cất trữ hóa.
- Các bao bì FeSO4 nên được dán biển báo hoặc tem cảnh báo nhắc nhở để đảm bảo một cách an toàn khi tiếp xúc.
Ngoài ra, khi chúng ta tiếp xúc với hóa chất này nên sử dụng găng tay hoặc đồ bảo hộ thích hợp.
Trên đây là toàn bộ thông tin liên quan đến FeSO4 có kết tủa không và tổng quan về FeSO4. Hy vọng bài viết này đã giải đáp được mọi thắc mắc của bạn về FeSO4 có kết tủa không. Theo dõi Chúng Tôi mỗi ngày để biết thêm nhiều thông tin hay và bổ ích nhé!
Trong chủ đề “FeSO4 có kết tủa không? Tính chất hóa học, vật lí Hóa học 12”, ta có thể kết luận như sau:
FeSO4, hay còn gọi là sunfat sắt (II), là một hợp chất hóa học quan trọng và phổ biến. Trong điều kiện bình thường, FeSO4 tồn tại dưới dạng một tinh thể màu trắng hoặc xanh lục, có phân tử khối là 278,02 g/mol. Nó có tính hút ẩm và dễ chảy trong không khí độ ẩm.
Tính chất hóa học của FeSO4 phụ thuộc vào việc nó được hòa tan trong nước hay không. FeSO4 cũng có khả năng tạo kết tủa ở một số điều kiện nhất định. Khi được hòa tan trong nước, FeSO4 tạo thành cation Fe2+ và anion SO42-, tạo ra dung dịch màu xanh lục. FeSO4 cũng có khả năng tạo ra kết tủa trắng khi kết hợp với một số nguyên tố, như hydroxit (Fe(OH)2) hoặc sunfat (FeSO4.7H2O).
Tuy nhiên, khi nhiệt độ tăng lên, FeSO4 dễ mất nước và chuyển thành dạng không màu, gọi là FeSO4.H2O hay FeSO4.Đạm. FeSO4 cũng có tính chất oxi hóa mạnh và có thể tác động như một chất tạo phức.
Tóm lại, FeSO4 có khả năng tạo kết tủa ở một số điều kiện và có tính chất hóa học và vật lí đa dạng. Chúng ta cần nghiên cứu kỹ hơn về tính chất của FeSO4 để hiểu rõ hơn về ứng dụng và tác dụng của hợp chất này trong lĩnh vực hóa học và các ngành khoa học khác.
Cảm ơn bạn đã xem bài viết FeSO4 có kết tủa không? Tính chất hóa học, vật lí Hóa học 12 tại Thcslytutrongst.edu.vn bạn có thể bình luận, xem thêm các bài viết liên quan ở phía dưới và mong rằng sẽ giúp ích cho bạn những thông tin thú vị.
Từ Khoá Liên Quan:
1. FeSO4
2. Kết tủa FeSO4
3. Tính chất hóa học FeSO4
4. Tính chất vật lí FeSO4
5. Phản ứng của FeSO4
6. FeSO4 tan hay kết tủa
7. Công thức hóa học FeSO4
8. Đặc điểm vật lí của FeSO4
9. Cách tạo kết tủa FeSO4
10. Sự tan trong nước của FeSO4
11. Phân tử FeSO4
12. Tính chất hoá học và vật lí của FeSO4
13. Tác dụng của FeSO4 trong môi trường axit
14. FeSO4 có phản ứng với dung dịch NaOH không?
15. FeSO4 có màu gì?


