Bạn đang xem bài viết Tính chất hóa học của phenol là gì? Dấu hiệu ngộ độc phenol tại Thcslytutrongst.edu.vn bạn có thể truy cập nhanh thông tin cần thiết tại phần mục lục bài viết phía dưới.
Phenol là một hợp chất hữu cơ có tính chất hóa học độc đáo và đa dạng. Với công thức là C6H6O, phenol được biết đến là một chất lỏng không màu có mùi thơm khá đặc trưng. Tính chất hóa học của phenol là một chủ đề nổi bật trong lĩnh vực hóa học, vì nó không chỉ có ứng dụng trong các ngành công nghiệp mà còn có tác động tiêu cực đến sức khỏe con người và môi trường.
Về tính chất hóa học, phenol có khả năng tạo ra nhiều phản ứng quan trọng. Đặc biệt, nó được biết đến như một chất tạo axit mạnh. Phenol có khả năng tác dụng với các chất bazơ, tạo thành các muối phenolat. Ngoài ra, nó cũng có thể tạo phức với các kim loại như natri, kali và nhôm.
Một trong những khía cạnh quan trọng cần lưu ý về phenol là tính độc. Ngộ độc phenol có thể xảy ra thông qua tiếp xúc da, hít phải hoặc tiếp xúc qua đường tiêu hóa. Dấu hiệu ngộ độc phenol có thể bao gồm việc xuất hiện các triệu chứng như đau đầu, buồn nôn, tình trạng loạn thần và trong trường hợp nghiêm trọng hơn, có thể gây tử vong.
Do đó, đối với tính chất hóa học của phenol, việc hiểu rõ và đảm bảo an toàn trong quá trình sử dụng và tiếp xúc là điều cần thiết. Công nghiệp và các lĩnh vực liên quan cần đưa ra các biện pháp phòng ngừa và kiểm soát nguồn gốc để đảm bảo tính an toàn cho con người và môi trường.
Trong sản xuất, phenol rất được trọng dụng trong các ngành sản xuất. Thế nhưng nó lại bị nghiêm cấm sử dụng trong chế biến thực phẩm bởi các tính chất hóa học của phenol rất độc hại. Vậy tính chất hóa học của phenol là gì? Đừng bỏ qua bài viết này của Chúng Tôi nếu muốn biết câu trả lời nhé!
Phenol là gì?
Phenol là gì?
Phenol là một hợp chất hữu cơ thơm trong hóa học. Phenol có công thức phân tử là C6H5OH. Cứ một phân tử phenol bao gồm một nhóm phenyl (−C6H5) liên kết với một nhóm hydroxyl (-OH).
Nhìn chung, phenol là một loại hóa chất độc hại. Bởi những tính chất hóa học của phenol xảy ra các phản ứng rất mạnh mẽ. Do đó, phenol bị cấm dùng trong thực phẩm.
Không chỉ vậy, phenol thiên về tính axít. Nó có thể gây bỏng nặng khi rơi vào da.
Phân loại phenol
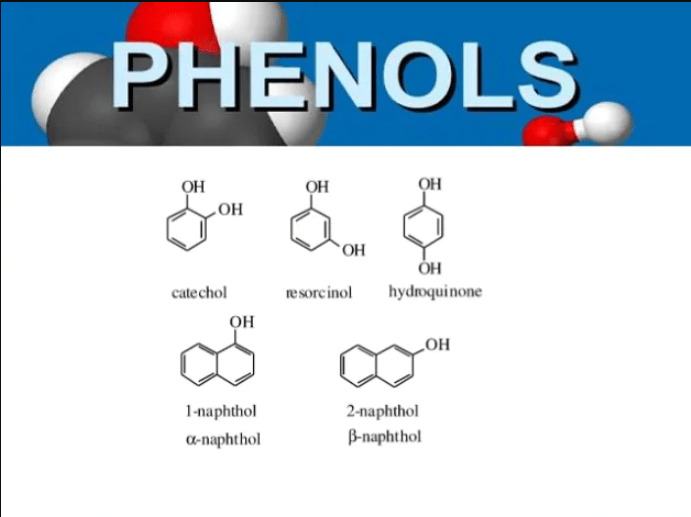
Phenol được phân thành hai loại chính nhờ số lượng nhóm -OH trong phân tử.
Monophenol
Những phenol mà phân tử có chứa 1 nhóm -OH thì phenol thuộc loại monophenol.
Ví dụ: phenol, o-crezol, m-crezol, p-crezol,…
Poliphenol
Những phenol mà phân tử có chứa nhiều nhóm OH thì phenol thuộc loại poliphenol.
Ví dụ: catechol, rezoxinol, hidroquinon,…
Có thể bạn không biết, các tính chất hóa học của phenol phần lớn đều dựa vào những gốc -OH có trong phân tử.
Tính chất hóa học của phenol
Tính chất hóa học của phenol gồm 3 đặc tính chính mà Chúng Tôi sẽ phân tích ngay sau đây.
Tính chất của nhóm -OH
Trong công thức hóa học của phenol có nhóm -OH. Do dó, tính chất hóa học của phenol có phần nào giống một bazo thông thường bao gồm:
Phenol tác dụng với kim loại kiềm
C6H5OH + Na → C6H5ONa + 1/2H2
Phản ứng này thông thường dùng để phân biệt phenol với anilin. Hay nói cách khác, ta có thể phân biệt anilin với phenol nhờ vào đặc tính nhóm -OH trong các tính chất hóa học của phenol.
Phenol tác dụng với bazo mạnh
Khi phenol tác dụng với bazo mạnh sản phẩm tạo thành sẽ là muối phenolate.
C6H5OH + NaOH → C6H5ONa + H2O
Phản ứng này dùng để tách phenol khỏi hỗn hợp anilin và phenol. Sau đó phenol được thu hồi lại nhờ phản ứng với các axit mạnh hơn.
Tính chất của nhân thơm – Phản ứng thế H ở vòng benzen
Thế Brom
Phenol tác dụng với dung dịch brom tạo 2,4,6 – tribromphenol kết tủa trắng. Phản ứng này dùng để nhận biết phenol khi không có mặt của anilin.
Phenol tham gia phản ứng thế brom dễ hơn benzen do có nhóm OH đẩy e làm tăng mật độ electron trong vòng benzen.
Thế Nitro
Phenol tác dụng với HNO3 đặc có xúc tác H2SO4 đặc, nóng tạo 2,4,6 – trinitrophenol (axit picric)
C6H5OH + 3HNO3 → C6H2(NO2)3OH + 3H2O
Không chỉ vậy, ngoài phenol thì tất cả những chất thuộc loại phenol đều có thể tham gia vào 2 phản ứng thế brom và thế nitro. Với điều kiện các loại phenol đó có nguyên tử H ở vị trí o, p so với nhóm OH
Phenol và phản ứng tạo nhựa phenolfomandehit
Trong môi trường axit tạo sản phẩm là nhựa phenolfomandehit, phương trình phản ứng như sau:
nC6H5OH + nHCHO → nH2O + (HOC6H2CH2)n
Bài viết liên quan:
- Tổng hợp 5 tính chất hóa học của bazơ bạn nên biết
- Tính chất hóa học của kim loại? 6 ứng dụng kim loại phổ biến nhất
- Tính chất hóa học của oxit? Khái quát về 4 loại oxit đặc trưng
Tính chất vật lý của phenol
Bên cạnh việc biết được tính chất hóa học của phenol, bạn cần nắm rõ các tính chất vật lý của nó.
Phenol là chất rắn, rất độc. Phenol để trong không khí sẽ hấp thụ độ ẩm và chảy rữa. Do đó, khi để lâu ở nhiệt độ phòng, phenol sẽ chuyển thành màu hồng.
Phenol ít tan trong nước lạnh, tan nhiều trong nước nóng nên dùng để tách bằng phương pháp chiết.

Cách điều chế, ứng dụng của phenol
Cách điều chế phenol
Để ứng dụng được các tính chất hóa học của phenol, trước tiên bạn phải biết cách điều chế chúng. Có hai cách phổ biến nhất để điều chế phenol như sau:
Điều chế phenol từ benzen
C6H6 → C6H5Cl → C6H5ONa → C6H5OH
C6H6 → C6H5CH(CH3)2 → C6H5OH
Điều chế phenol từ nhựa than đá
Đầu tiên cho nhựa than đá + NaOH dư.
Sau đó, chiết để lấy lớp nước có C6H5ONa.
Cho C6H5ONa + H+ → C6H5OH.
Ứng dụng của phenol
Nhờ tính chất hóa học của phenol rất đặc biệt và cách điều chế cùng vô cùng đơn giản nên nó được ứng dụng trong nhiều ngành khác nhau. Chúng Tôi sẽ đưa đến bạn các công dụng của phenol trong nhiều lĩnh vực như sau:
- Công nghiệp chất dẻo: phenol là nguyên liệu quan trọng để điều chế nhựa phenol formaldehyde.
- Công nghiệp tơ hóa học: Có thể dùng phenol để tạo ra tơ polyamide.
- Nông dược: Phenol điều chế được chất diệt cỏ dại và kích thích tố thực vật 2,4 – D (đây là muối natri của axit 2,4 điclophenoxiaxetic).
- Nông phẩm: Phenol cũng là nguyên liệu thiết yếu để điều chế một số phẩm nhuộm, thuốc nổ (axit picric).
Không chỉ vậy, nhờ tính diệt khuẩn vượt trội của phenol, nên phenol còn được dùng để trực tiếp làm chất sát trùng, tẩy uế. Hoặc dùng phenol để điều chế các chất diệt nấm mốc (ortho – và para – nitrophenol…). Hai ứng dụng này có thể sử dụng linh hoạt trong nhiều ngành.
Những lưu ý khi sử dụng phenol
Dấu hiệu bị ngộ độc phenol
Như đã nói, các tính chất hóa học của phenol rất mạnh mẽ. Vì thế khi con người tiếp xúc với nó phải vô cùng cẩn thận. Khi xảy ra các dấu hiệu sau thì phải ngay lập tức đến bệnh viện vì rất có thể bạn đã bị ngộ động phenol.
- Khi bạn cảm thấy da khó chịu
- Mắt và màng niêm mạc trở nến đau nhói, không thấy được gì
- Thở không đều, yếu cơ và run cơ.
- Co giật, mất phối hợp tứ chi
- Hôn mê và ngừng hô hấp là điều nghiêm trọng nhất khi hít phải phenol ở liều gây chết người.
Lưu ý khi sử dụng phenol
Chính vì những nguy hiểm do tính chất hóa học của phenol đem lại, bạn cần lưu ý những điều sau khi sử dụng:
- Tuyệt đối không để phenol tiếp xúc trực tiếp với cơ thể.
- Mỗi khi sử dụng cần có các biện pháp bảo hộ cần thiết theo quy định như bao tay, kính chắn, đồ bảo hộ,…
- Không được cố ý hít hoặc nuốt phenol.
Nếu vô tình để phenol dính vào mắt hoặc da thì phải rửa ngay với nhiều nước. Rửa liên tục ít nhất trong 15 phút và đến ngay cơ sở y tế để được kiểm tra và chữa trị kịp thời.

Mua phenol ở đâu an toàn, uy tín?
Để sử dụng những chất dung môi công nghiệp như phenol bạn cần lựa chọn những nơi uy tín trên thị trường. Phenol nguyên chất và được đảm bảo sẽ có ứng dụng cao hơn và đáp ứng được các yêu cầu trong sản xuất.
Bạn có thể mua phenol ở:
- Khu vực Hà Nội: Tại số 9 Ngõ 51, Lãng Yên, Hai Bà Trưng – Hà Nội.
- Khu vực Hồ Chí Minh: Tại phòng số 301A, tòa nhà WINHOME số 91-93 Đường số 5, Phường An Phú, Quận 2, thành phố Hồ Chí Minh.
- Khu vực Cần Thơ: Tại K2-2, Võ Nguyên Giáp, phường Phú Thứ, quận Cái Răng, thành phố Cần Thơ.
- Nhà máy Văn Lâm – Hưng Yên.
- Kho Hải Hà: Lô CN5.2Q, Khu hóa chất hóa dầu, KCN Đình Vũ, Đông Hải 2, Hải An, Hải Phòng.
Nắm rõ các tính chất hóa học của phenol sẽ giúp bạn nhận biết tầm quan trọng của nó các ngành công nghiệp. Bên cạnh đó, hãy cẩn thận khi sử dụng phenol khi nó có thể gây chết người. Đừng quên cập nhật các kiến thức khác qua các bài viết sau của Chúng Tôi nhé!
Tính chất hóa học của phenol được xem là khá đặc biệt và có nhiều ứng dụng quan trọng trong lĩnh vực hóa học và công nghiệp. Phenol có công thức phân tử C6H6O, là một hợp chất hữu cơ với nhóm chức hydroxyl (OH) gắn với hoạt động tăng, đóng vai trò quan trọng trong nhiều phản ứng hóa học.
Phenol có tính chất axit, khả năng tạo các liên kết hydrogen và làm mất cân bằng trong phản ứng. Ngoài ra, nó cũng thể hiện tính chất oxi hóa mạnh, có khả năng tác động mạnh lên môi trường. Điều này có thể dẫn đến nguy cơ ngộ độc phenol.
Ngộ độc phenol thường xảy ra thông qua tiếp xúc da, hít phải hoặc nuốt phải các sản phẩm chứa phenol. Dấu hiệu ngộ độc phenol có thể bao gồm: da và niêm mạc bị cháy, đỏ hoặc sưng, khó thở, ho, nôn mửa, tiêu chảy hoặc táo bón, và có thể gây tổn thương nội tạng nghiêm trọng như thận và gan.
Vì vậy, việc tiếp xúc với phenol cần được thực hiện cẩn thận, đặc biệt với các sản phẩm chứa phenol trong môi trường công nghiệp. Để tránh nguy cơ ngộ độc, người ta phải tuân thủ các biện pháp an toàn, bao gồm sử dụng thiết bị bảo hộ như mặt nạ, găng tay và quần áo bảo hộ.
Tóm lại, tính chất hóa học của phenol là có tính axit, tạo liên kết hydrogen, và có tính chất oxi hóa mạnh. Ngộ độc phenol có thể xảy ra qua tiếp xúc da, hít phải hoặc nuốt phải, và dẫn đến những dấu hiệu đặc trưng. Việc tiếp xúc với phenol cần được thực hiện cẩn thận để tránh nguy cơ ngộ độc.
Cảm ơn bạn đã xem bài viết Tính chất hóa học của phenol là gì? Dấu hiệu ngộ độc phenol tại Thcslytutrongst.edu.vn bạn có thể bình luận, xem thêm các bài viết liên quan ở phía dưới và mong rằng sẽ giúp ích cho bạn những thông tin thú vị.
Từ Khoá Liên Quan:
1. Tính axit của phenol
2. Tính bazơ của phenol
3. Điều chế phenol từ benzene
4. Phản ứng trái pha của phenol
5. Phản ứng oxi hóa của phenol
6. Phản ứng khử của phenol
7. Phản ứng chuyển hóa của phenol
8. Tính chất oxi hóa của phenol
9. Tính chất khử của phenol
10. Tính chất chống oxy hóa của phenol
11. Tác dụng với axít của phenol
12. Tác dụng với bazơ của phenol
13. Phản ứng ester hóa của phenol
14. Phản ứng eter hóa của phenol
15. Phản ứng amin hóa của phenol


